5:後遺症
PAGE CONTENTS
排尿障害
前立腺がんの後遺症としての排尿障害には主に次の3つが考えられます。
①排尿困難(尿が出にくい)・・・小線源療法やHIFUの後で起こりやすい
手術(全摘)でも排尿困難が生じることがあります
②頻尿・切迫尿・・・外部照射中およびその後
③尿漏れ、尿失禁・・・手術(全摘)の後
前立腺がんの全摘術を受けた場合、ほとんどの人が尿失禁を体験します。
ただ、これらは数週間から1年以内に改善されることがほとんどで、
たとえ排尿障害が残ったとしても、なんとか許容限度内に納まっていることが多いのですが、
中にはいつまでたってもひどい尿漏れが継続する高度の排尿障害に悩まされている人もおられます。
放射線治療に伴う合併症は、ほとんど一時的であるため、少し不自由を味わうだけで済んでしまいますが、
血尿(膀胱の炎症)や血便(腸の炎症)などの晩期後遺症が出た場合は、簡単には治らずなかなかやっかいです。
軽度〜中等度の排尿障害
膀胱や尿道を支える骨盤底筋や尿道括約筋の機能が低下して起こる腹圧性尿失禁には、骨盤底筋を鍛える体操が有効で、
軽度ならこれだけも治る場合がめずらしくありません。
外尿道括約筋を締めるβ2作動薬(スピロペントetc)が有効な場合もあります。
切迫性尿失禁は、尿が十分たまっていないのに膀胱の異常収縮により急にトイレに行きたくなる過活動膀胱の人に起こりやすく、
抗コリン薬やβ3作動薬が有効とされています。
軽度の場合は、適宜、尿パッドや失禁パンツなどのケアアイテムを用い、治療・訓練を続けるうちに数週間から数カ月で治るものがほとんどです。
薬が効きにくい軽度〜中度の排尿障害では、装着型収尿器やペニクランプを用いたり、コラーゲン注入術や
スリング術を行うこともあります。
切迫性尿失禁でも薬が効きにくいものに対しては、欧米では仙骨神経刺激療法(SNM)が用いられていますが、
日本ではまだ保険適用となっていません。
(SNMは便失禁に対しては2014年に保険適用となりました)
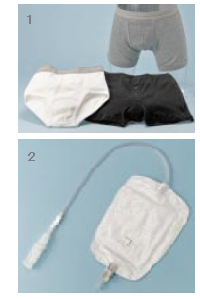
尿パッド・失禁パンツ
ズレを予防できる男性専用パッドはほとんどないので、男女共用型を失禁量に合わせて使用する。(写真は男性用パッドの一例)
失禁パンツ(図-1)は、前側に吸収体が入っていて、30mL以内の少量の漏れに対応できる。
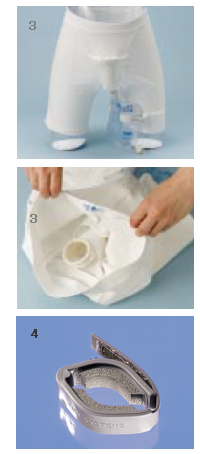
装着型収尿器
使い捨てタイプ(図-2)は、直接ペニスに付けるので、長時間付け続けるとスキントラブルを起こ
す可能性がある。
再利用タイプ(図-3)は、パンツ内に固定された受尿器に逆流防止弁の付いたチューブ部分が接続されている。
スキントラブルはこのほうが少ない。
受尿器は、排泄姿勢により、一人ひとりに適したタイプが選べる。
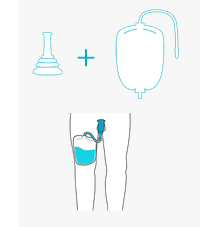
ペニクランプ
ペニスを挟み、漏れを防ぐ用具(図-4)です。簡便に使用でき、漏れその
ものを抑えることができますが、少なくとも2〜3時間ごとにペニスを解放する必要がある。
長時間、使用しているとうっ血を起こす可能性があるので、自己管理ができることが使用条件の一つ。
切迫性尿失禁で膀胱の収縮が激しい患者には適しない。
コラーゲン注入術 (医療保険適用あり)
内視鏡を使い尿道粘膜の下にコラーゲンを注射する方法。
比較的簡単で合併症も少ないが、確実性と持続性に欠けるのが欠点。
(尿道)スリング術 (医療保険適用あり)
外尿道括約筋の機能がある程度残っており、
腹圧時に尿道が後方にぐらつくタイプの尿失禁で、失禁量が200-300g/日 程度までの軽〜中度の排尿障害に対しては、
尿道を恥骨側に人工テープで吊り上げる「スリング術」によりしばしば症状の改善がみられる。
女性の尿失禁にはこの「ぐらぐら型」が多いので、スリング術が広く用いられているが、全摘術後の尿失禁に対しては確実性は乏しい。
ただし、自然排尿ができるのが利点。
外部装着型収尿器
<コンドーム型>
ペニスに直接装着する収尿器で、集められた尿は脚に装着された蓄尿袋に溜められます。
蓄尿袋は上腿や下腿など、体の動きを妨げない位置に固定でき、服の上からは比較的目立ちにくい。
収尿器の交換は1日1回程度なので、おむつのような頻繁な交換が必要ないのが利点。
メーカーは多数ありますが一例を示しておきます。
http://uric30.com/
<レシーバー型>
ペニスに密着させず、緩くかぶせて受け取る方式なので、サイズ選びの煩わしさがなく、装着感も楽。
ただ、動きへの追随に限界があるので、外出程度は大丈夫だが、はげしい運動には不向き。
高度排尿障害・・・人工尿道括約筋
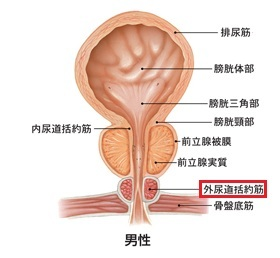
排尿のコントロールは主として外尿道括約筋(左図参照)で行われ、膀胱頸部の内尿道括約筋が
それを補佐しています。
前立腺がんの場合、全摘除術後の排尿障害は付きものと言っても過言ではありませんが、
これらのほとんどは一時的なものか、もしくは障害が残ってもなんとか我慢できる程度に留まっています。
しかしながら、約1〜3%の患者は、手術時に外尿道括約筋を損傷するなどして、
(いわゆる手術ミスもあれば、浸潤状態により止むなくそうなるケースもある)
尿道の締め付けが物理的に難しくなり、
多量かつ頻繁な尿漏れが継続する、いわゆる「ゆるゆる型」の高度排尿障害に悩まされます。
おむつの常用が欠かせず(年間の出費が数十万!)、外出もままならず、ひきこもりから鬱を発症する人もめずらしくありません。
こうした高度排尿障害の患者は年間数百人と見られていますが、男性尿失禁治療に習熟している医師、医療機関は極めて少なく、
自分に適した治療法を知る機会もないまま見放されてきたのがこれまでの実情でした。
骨盤底筋を鍛える体操や薬物療法が無効で、外尿道括約筋の機能が損なわれていると思われる高度尿失禁(400g/日が目安)に対する
唯一効果的な治療法は「人工尿道括約筋」の埋込み手術です。
埋め込んだ後も、創部の安定までに約一月半を有し、その間使用を控えなければならないのが欠点ですが、
半数近くの患者でほぼ失禁がなくなり、ほとんどの人(約9割)が生活に支障がない程度に尿失禁が軽減するという治療法。
米国ではすでに30年以上の実績を有し、我国でも2012年4月より保健適用が認められました。
重度の尿失禁に悩む人にとっては大きな朗報でなり、人工尿道括約筋の普及にもこれではずみがつくと思われます。
人工尿道括約筋の埋め込み術は全身麻酔下で行われ、手術の所要時間は1〜2時間。
入院期間も1週間弱で外見上装着の有無もわかりません。
また、感染や機器の初期不良さえなければ長期間の継続利用が可能で、国内のデータでも10年間継続利用している患者の割合が7割を超えています。
激しい運動も可能で、少量の尿漏れや尿滴下がある以外、尿失禁は認められなくなります。
人工尿道括約筋を開発した米国のAMS社によると、これまでこの治療を受けた患者は、全世界で13万人に上るということです。
人工尿道括約筋の治療を行っている施設はこちらのサイトから
重い尿失禁にお悩みの方に 〜人工尿道括約筋という選択肢〜
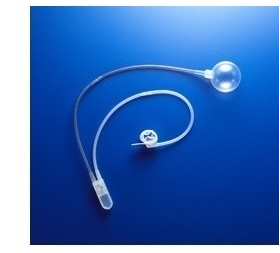
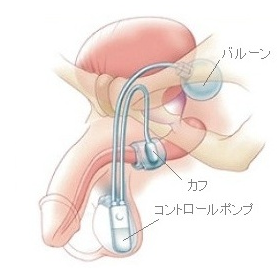
人工尿道括約筋のしくみ (左図参照)
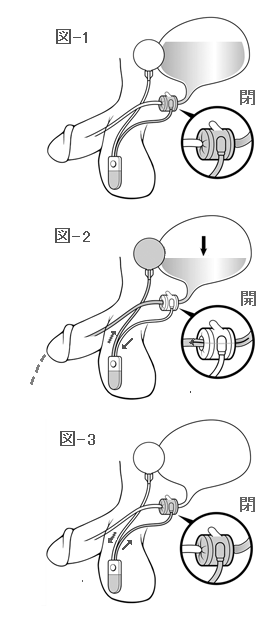
【図-1】
通常はカフに循環液(生理食塩水)が満たされ尿道を締め付けているので、膀胱内に尿が溜まる。
【図-2】
陰嚢内のコントロールポンプを押すと、カフ内の循環液がバルーンに移動し、
カフが緩んで排尿が可能となる。
【図-3】
排尿終了後は、数分で自動的にバルーンの循環液がカフに移動し、また尿道を締め付ける。
性機能障害
リンパ浮腫
鼠径(そけい)ヘルニア